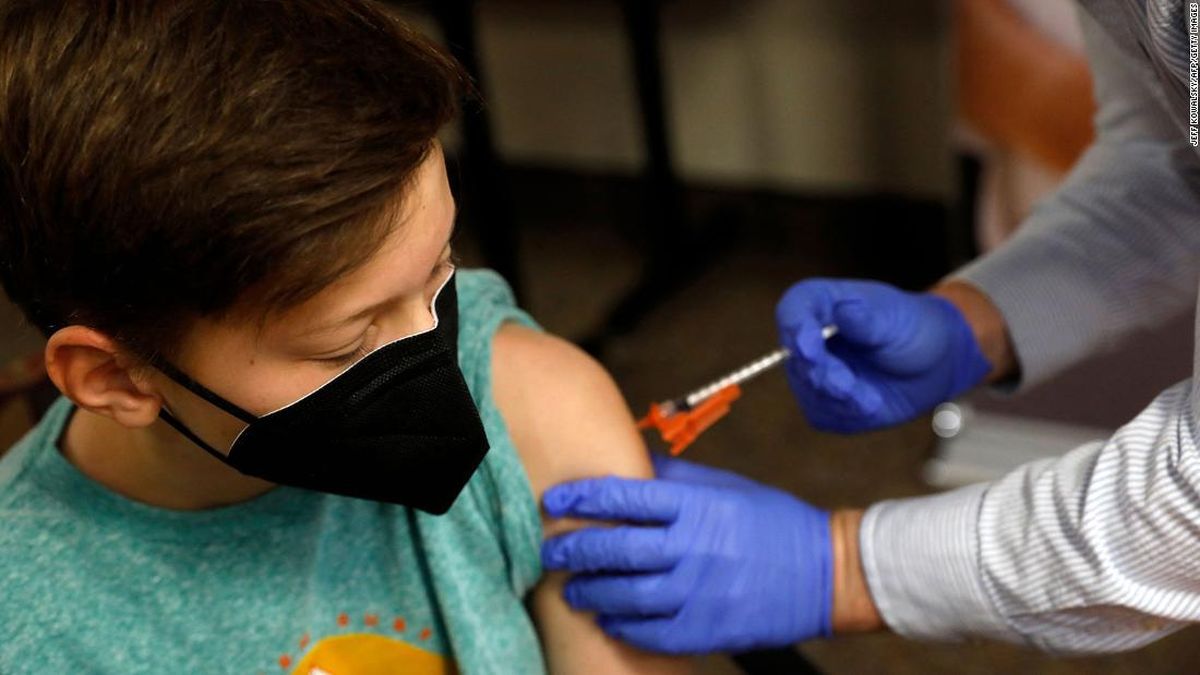
El 13 de octubre, cuando aún no había estallado el escándalo sobre los dichos de la ministra de Salud nacional, Carla Vizzotti, sobre la vacuna de fabricación china Sinopharm, el Concilio de Naciones Unidas por la Vida y la Verdad elevó un pedido de informes a la cartera de Salud y a la Asociación Argentina de Pediatría. Las respuestas oficiales sembraron dudas y temor.
El pedido, firmado por la presidente del Concilio Elizabeth Marquez, incluyó ver los papers científicos sobre los que se respaldó la decisión de inocular la vacuna Sinopharm en niños de tres a once años, los resultados de los ensayos realizados de las fases 1, 2 y 3, y los informes sobre las reacciones adversas de la vacuna en adultos. Además, se pidió que se indique la tesitura oficial frente a la publicación de la OMS en la que el organismo internacional no recomienda administrar esa vacuna en menores de dieciocho años.
La respuesta oficial, que llegó el 25 de octubre a través de un comunicado publicado en el Boletín Oficial por la dirección nacional de Control de Enfermedades Transmisibles, llegó plagada de evasivas y sin datos concretos, lo que elevó nuevamente la preocupación por las políticas del gobierno nacional respecto al plan de vacunación.
La dirección nacional aseguró que la aprobación de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) se basó en “datos proporcionados por los diferentes laboratorios en cuanto a los resultados de eficacia, seguridad e inmunogenicidad”. Sin embargo, no aclaró cuáles fueron los laboratorios que intervinieron ni incluyó la publicación de los resultados.
La respuesta oficial, que llegó el 25 de octubre a través de un comunicado publicado en el Boletín Oficial por la dirección nacional de Control de Enfermedades Transmisibles, llegó plagada de evasivas y sin datos concretos, lo que elevó nuevamente la preocupación por las políticas del gobierno nacional respecto al plan de vacunación.
La dirección nacional aseguró que la aprobación de la Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) se basó en “datos proporcionados por los diferentes laboratorios en cuanto a los resultados de eficacia, seguridad e inmunogenicidad”. Sin embargo, no aclaró cuáles fueron los laboratorios que intervinieron ni incluyó la publicación de los resultados.